Se inició la prueba en humanos del suero equino hiperinmune desarrollado en la Universidad de San Martín (UNSAM). El estudio contempla la participación voluntaria de 242 pacientes adultos con enfermedad moderada a severa causada por SARS-CoV-2 y confirmada por PCR. La semana pasada, la Administración Nacional de Medicamentos, Alimentos y Tecnología Médica (ANMAT) aprobó el ensayo clínico.
Se trata de un tratamiento avanzado contra la covid-19 que empezó en el Sanatorio Güemes y que también se aplicará en el Hospital General de Agudos Dr. Ignacio Pirovano, ambos de CABA, en el Hospital Cuenca Alta – SAMIC de Cañuelas y en el Instituto Médico Platense de La Plata. Se prevé sumar diez centros más.
El doctor Fernando Goldbaum, quien encabeza el equipo que lidera el tratamiento, explicó las características del proyecto. «El virus necesita, para entrar a las células, replicarse. Para ello debe reconocer el receptor, unirse a la célula y entrar. Entonces, lo que hicimos fue tomar esa proteína, ese pedacito de virus, lo producimos en gran cantidad por un proceso biotecnológico, inmunizamos a caballos (proceso inocuo para los animales) y ellos producen una gran cantidad de anticuerpos con esa proteína, que es como la llave. Esos anticuerpos neutralizan a la llave e impide que el virus pueda entrar a las células», indicó en declaraciones al canal C5N.
«Los médicos e investigadores van a ofrecer este tratamiento a pacientes de moderados a graves con menos de diez días de evolución de la enfermedad, porque ya se ha demostrado a través del plasma de convalecientes que cuanto más temprano se apliquen los anticuerpos, más probabilidad de que estos neutralicen la replicación viral», detalló el director científico de Inmunova e investigador superior del CONICET, dos entidades que lideran el desarrollo.
Desde la UNSAM señalaron que el suero anti-covid-19 es el primer potencial medicamento innovador para el tratamiento de la infección por el nuevo coronavirus totalmente desarrollado en Argentina. «Es un tratamiento para pacientes con diagnóstico de la infección, a ser administrado en las primeras etapas de la enfermedad, que ya demostró que es capaz de neutralizar al virus en pruebas de laboratorio», aseguraron.
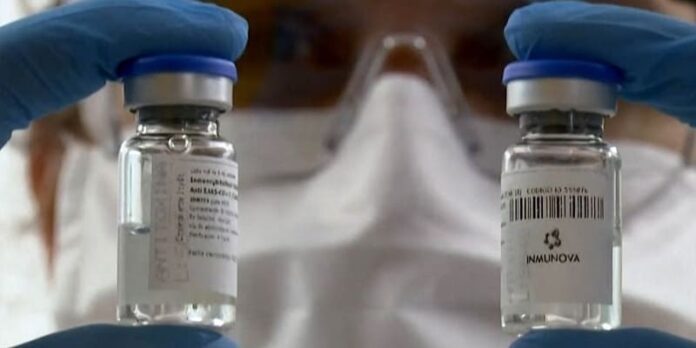
El suero terapéutico desarrollado por @inmunova , empresa incubada en la UNSAM, es una inmunoterapia basada en anticuerpos policlonales equinos, obtenidos mediante la inyección de una proteína recombinante del SARS-CoV-2 en estos animales. Lee mas acá: https://t.co/1joFBH53Ao pic.twitter.com/bGfuVgoLK7
— Universidad Nacional de San Martín (@unsamoficial) July 27, 2020
De ahora en más, las pruebas apuntan a demostrar la seguridad y eficacia del suero hiperinmune en términos de mejoría clínica del paciente, es decir, la recuperación pronta para poder ser externado, que no avance la enfermedad y por tanto la necesidad de asistencia respiratoria mecánica o el traslado a una unidad de cuidado intensivo.
«Si bien las vacunas son la estrategia ideal, la pandemia plantea la necesidad de terapias efectivas en plazos más próximos que permitan disminuir el impacto del nuevo coronavirus. Nuestro suero no necesita de donantes, se puede producir en grandes cantidades y se puede suministrar a cada paciente en una concentración conocida de anticuerpos», agregó Goldbaum.
«El suero equino tiene una capacidad neutralizante de veinte a cien veces mayor que el promedio del plasma de convalecientes», detalló el investigador. «La capacidad de neutralizantes es mayor, se los puede producir en gran cantidad por los volúmenes que se pueden obtener y se puede escalar para producir una cantidad muy importante, lo que permitiría utilizar estos anticuerpos en etapas más tempranas de la enfermedad», puntualizó.
Además del trabajo articulado entre la UNSAM y el laboratorio Inmunova, también participan del desarrollo el Instituto Biológico Argentino (BIOL), la Fundación Instituto Leloir (FIL), Mabxience, el CONICET, ANLIS Malbrán y el Instituto de Virología Dr. José M. Vanella de la Universidad Nacional de Córdoba.
Hay más de 15.000 voluntarios anotados para probar la vacuna
Las pruebas de la vacuna elaborada por las compañías Pfizer y BionTech, que ya recibieron el aval de la ANMAT, comenzarán la semana próxima y ya hay más de 15.000 voluntarios alistados, señaló el ministro de Defensa, Agustín Rossi.
Junto a los especialistas de las empresas trabajará un reconocido equipo argentino encabezado por el infectólogo Fernando Polack. El objetivo es establecer la eficacia de la vacuna que, según los antecedentes realizados en Estados Unidos y Alemania, permite desarrollar anticuerpos altos, al nivel de un enfermo recuperado.
Quienes quieran inscribirse como voluntarios deben tener entre 18 y 85 años y vivir en la Ciudad de Buenos Aires o a menos de 60 kilómetros de esta. No podrán hacerlo embarazadas o en periodo de lactancia. En el sitio web para postularse completan el formulario y luego son contactados.
En Estados Unidos y Alemania la vacuna recibió la aprobación del examen de seguridad y toxicidad, por los respectivos organismos oficiales a cargo de esa tarea, de modo que ahora continuarán las pruebas. Se aplicarán dos dosis en un periodo de tres semanas entre cada una. A pesar de que la vacuna ya superó las fases de control 1 y 2, habrá un seguimiento del avance de los voluntarios, con el fin de detectar posibles efectos adversos.